CE��֤�������ж�һ��ҽ����е��ȷ�ķ��࣬��ƾ��е�������Dz����ģ�����֪��������Ԥ��ʹ��Ŀ�ģ�Intended Purpose ��!
���Ǿ�������������һ�仰���⣺ijij��Ʒ��CE���������ڼ���ҽ����е��
������Ҳ����֪������һ��ҽ����е�����ƶ��ж���CE��֤�����еķ��ྭ���Dz�����!
- ŷ��������������
ŷ����������ҽ����е�ķ����кܴ�IJ�ͬ��
������FDA��ҽ����е������ͨ�õ��ص������Ѿ�������������һ�����������ݿ�ɲ�ѯ��
ŷ�����ǽ�����һ������������������ݲ�Ʒ��Ԥ��ʹ��Ŀ�ģ�Intended Purpose �����շ�������Լ����з�����
- ͬһ����Ʒ���ȿ�����ҽ����е��Ҳ���Բ���ҽ����е
��������һ����Ʒ�Ƿ�Ϊҽ����е ��ȫ��FDA������
��ŷ�ˣ�һ����Ʒ�Ƿ�Ϊҽ����е ��������(�����IJ�ƷԤ��ʹ��Ŀ��)����, ���磺������ȿ�����ҽ����е��Ҳ���Բ���ҽ����е��
- ͬһ����Ʒ�������Dz�ͬ����ҽ����е
���磺������������Ԥ��ʹ��Ŀ�IJ�ͬ��������ȿ�����I��ҽ����е��Ҳ������IIa��IIb��ҽ����е��
- ͬһ����Ʒ����Ϊϵͳ��һ����ʱ����Ϊ���ʱ���ڲ�ͬ�����
���磺�����������÷�����ʽ��ȡ��ˮװ�õ����������ʢ��ˮ����������Ϊϵͳ��һ����ʱ������IIa�࣬������Ϊ���ʱ�������I�ࡣ
- ���ƵIJ�Ʒ�������Dz�ͬ����ҽ����е
���磺X����Ƭʱ���õ�ͼ��ͨ��ϵͳPicture Archiving and Communication Systems (PACS)����ͬ������������Ԥ��ʹ��Ŀ(����)�IJ�ͬ��PACS������I��ҽ����е��Ҳ������IIa��IIb��ҽ����е��
- ���ƵIJ�Ʒ���е�����ҽ����еMD, �е����������������еIVD
���磺��Ѫ����� ������ʽ�Ļ�Ӵ���Ƥ���ģ�������MDD 93/42/EEC ָ���Ͻ�ģ���ͨ��ҽ����е MD��
��� �Ƿ�����ʽ�Ļ���ȫ�Ӵ�����Ƥ���ģ�������IVD 98/79/ec ָ���Ͻ�� ���������еIVD��
ҽ����еָ�� MDD 93/42/eec ��¼�����궨18������ҽ�Ʋ�Ʒ��Σ�ճ̶ȣ�����Ʒ��Ϊ���ࡢ��a�ࡢ��b�ࡢ���ࡣ
��Ʒ�������
1������Ӧ������е��Ԥ��ʹ��Ŀ�ľ�����
2�������е�Ǻ�������е���ʹ�ã��������ֱ�������ÿ����е��
3���������Ժ�����һ��ʹ�õ���е�ֿ��������ࣻ
4��������Ӱ��ij����е����������е����ͬһ���͡�
������
ʱ �䣺 ��ʱ ��<60���ӣ������ڣ�<30�죩�����ڣ�>30�죩
�����ԣ��Ǵ��ˡ�ͨ�������ˣ���ƴ��� ��ֲ�롣
����λ�ã�����ѭ����������ϵͳ�������ط���
������Ӧ����Դ����Դ��
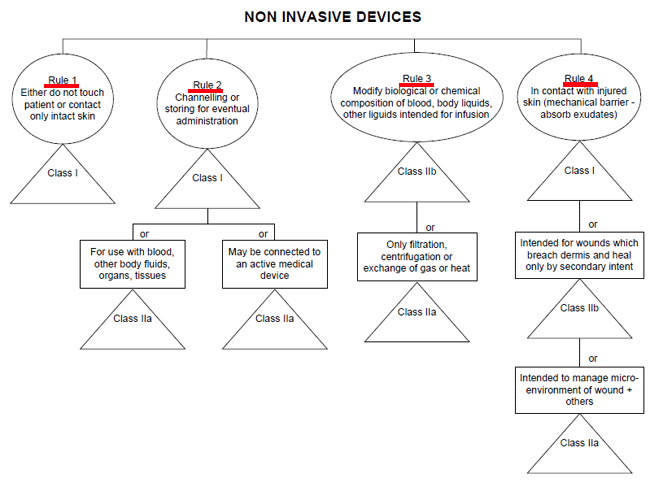
����1��4�����зǴ�������е������I�࣬�������ǣ�
���ڴ�����Һ(Ѫ������) II a��
��Ila���������͵���Դҽ����е�� II a��
�ı���Һ�ɷ� II a��II b��
һЩ�˿ڷ��� II a��II b��
����5�������������ҽ����е
��ʱʹ��(����ѹ�����ϡ��������) I��
����ʹ��(���ܡ������۾�) II a��
����ʹ��(��������) II b��
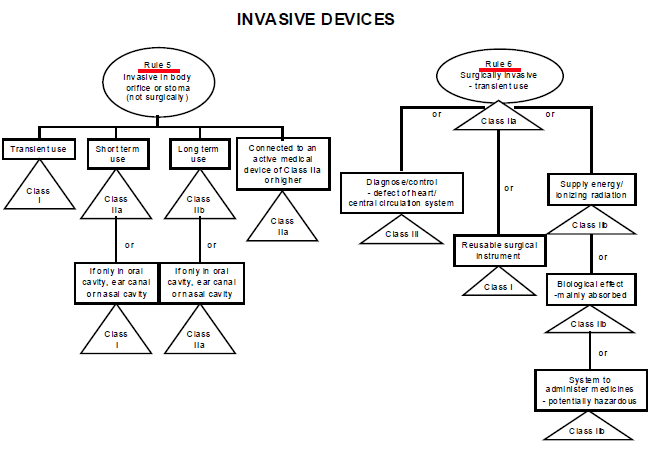
����6-8����ƴ�������е
��ʹ�õ������е(ǯ�ӣ�����) I��
��ʱ�����ʹ��(����롣�������) 11a��
����ʹ��(�ٹؽڣ����ھ���) II b��
������ѭ��ϵͳ(CCS)��������ϵͳ�Ӵ�����е III��
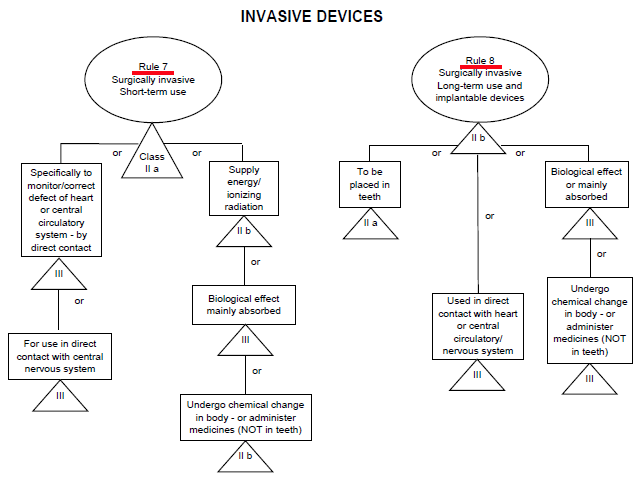
 ����9�������������������е II a�� ����9�������������������е II a��
������̼��������ꡢƤ�����ƻ�����������
һ��DZ��Σ�շ�ʽ������ II b��
��Ӥ�������䡢��Ƶ�絶��������ʯ����X�����
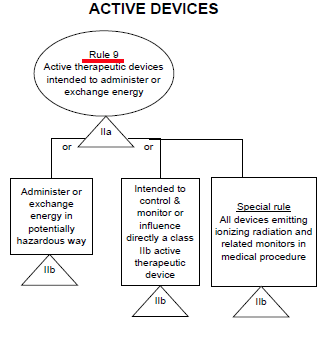
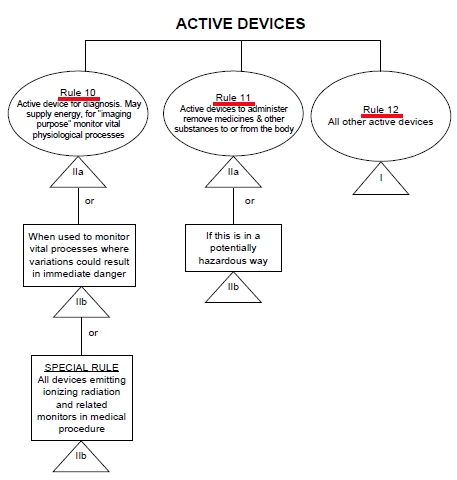
����10�������е
�ṩ����(�˴Ź����������) II a��
��ϣ��������ڷ���ҩ��ֲ� II a��
(r������������ӷ��������)
��ϣ�������������(�ĵ�ͼ���Ե�ͼ) II a��
Σ������¼����������� II b��
(�����е�Ѫ��������)
�����������(X���������) II b��
����11 ����ҩ����������ʽ����������Դ��е II a��
(�����豸��������)
����һ��DZ��Σ�շ�ʽ���� II b��
(������������������������ѹ����)
����12������������Դҽ����е����I��
(�۲�ơ������Ρ����Ρ����������Ƶơ���¼�����۲����ͼ���õ���Դ��е)
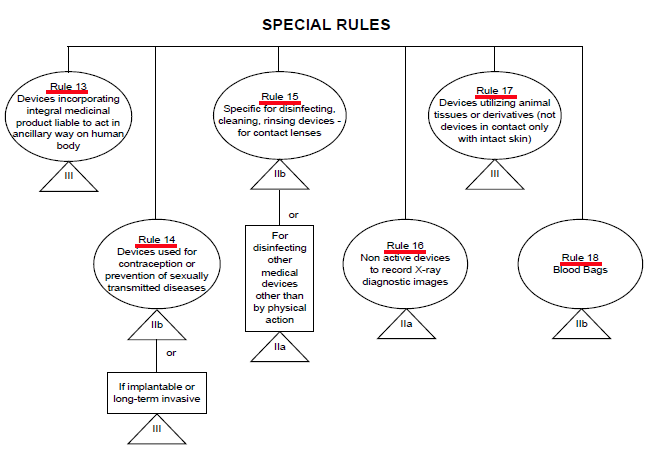
����13����ҽ�����ʽ�ϵ���е����ɱ���ӵı����ס��������ص�������ϣ� III��
����14�������þߣ������ס��ӹ�ñ II b�� �� II b/III�� (�ӹ��ڱ����� III��)
����15����ϴ����������е
ҽ����е(�ڿ�������) II a��
�Ӵ���(����Һ������Һ) II a��
����16�����ڼ�¼X����ͼ�����е(X��Ƭ) II a��
����17�����ö�����֯����е����������Ĥ�����ߡ���ԭ�� III��
����18��Ѫ�� II b��
|





